
资讯中心
作者:香雪生命科学
发布时间:2025-12-31
阅读:926
癌症是当下全球主要的死亡原因之一,近年来,由于饮食、环境、人口老龄化等因素,全球癌症负担不断增长,癌症作为主要死因的情况日益突出,对公共健康构成严重威胁。2025年10月发表于《柳叶刀》的研究论文(The Lancet. 2025)显示,全球癌症负担持续攀升,2023年,全球癌症新发病例约1850万例,死亡人数约1040万,预计到2050年,新发病例将激增至3050万,死亡人数将攀升至1860万,增幅分别为64.9%和78.8%。作为世界上的人口大国,中国的癌症数据不容乐观,中国国家癌症中心发布的最新数据(J Natl Cancer Cent. 2024)显示,2022年,中国癌症新发病例约482万例,死亡人数约257万,中国已经成为了名副其实的癌症大国,不论是新发人数还是死亡人数,中国都位居全球第一。
死亡人数全球第一的癌症:肺癌
世界卫生组织(WHO)下属国际癌症研究机构(International Agency for Research on Cancer,简称IARC)最新数据显示,肺癌是目前全球发病率和死亡率均排名第一的癌症,已连续十年位居全球癌症死亡率首位。
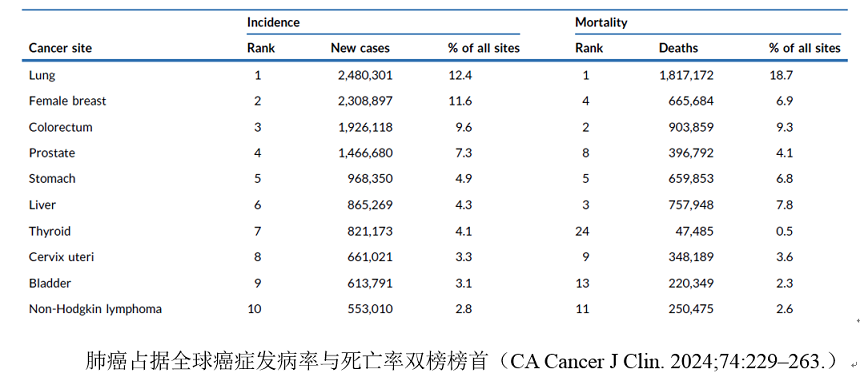
中国国家癌症中心发布的最新数据(J Natl Cancer Cent. 2024)显示,中国肺癌年新发病例数约为106万例,死亡病例数约为73万例,分别占全球肺癌年新发病例数(约248万)与死亡病例数(约182万)的42.7%与42.1%。中国人口(约14.1亿)占世界人口总数(约82.6亿)的17%。很明显,人数不到全球五分之一的中国,负担着全球超40%的肺癌发病数和死亡数,中国的肺癌发病率和死亡率远远高于世界平均水平。肺癌是全球死亡人数第一的癌症,更是中国癌症死亡的第一病因,是中国的“癌王”之一。
非小细胞肺癌是肺癌中最常见的类型,约占所有肺癌病例的85%。目前非小细胞肺癌治疗手段包括手术、放疗、化疗、靶向疗法、免疫疗法等。由于肺癌早期缺乏特异性症状,大多数的患者在确诊时已属晚期,失去手术治疗机会。近年来,尽管医疗技术有所进步,中国肺癌的五年总体生存率已有所提升,但肺癌依旧是中国正在面临的严峻的公共卫生问题。对于中晚期非小细胞肺癌患者一直以来都存在着巨大未被满足的临床需求,非常亟需开发新一代的治疗药物(如细胞治疗),以图提高治疗有效率,降低肺癌的死亡人数。
胰腺癌“癌王”的“王座”由何而来?
胰腺癌被称为“癌王”,不是因为它的发病数量,而是因为它在恶性程度、隐蔽性、治疗难度和极低的生存率等方面的综合表现。可以说肺癌是一个“量的癌王”, 胰腺癌是一个“质的癌王”,这是更加可怕的。来看中国的数据,肺癌的年死亡率/发病率之比约为0.69,而胰腺癌的年死亡率/发病率之比高达0.9,反映出其极差的预后。胰腺癌为何如此恐怖,因为它有以下特征:
1、深藏的“隐形杀手”。胰腺位于腹腔深处,胃的后方,被其他器官遮挡,常规体检(如B超)很难清晰发现早期病变;症状隐匿且不特异,早期几乎没有症状,即便出现腹痛、消化不良、腰背酸痛等,也极易被误诊为胃病或腰肌劳损,等出现黄疸、严重消瘦时,往往已到晚期。
2、生物学行为上的“暴君”。其一,侵略性强,胰腺癌细胞生长迅速,周围有丰富的血管和淋巴管网,极易发生局部侵犯和远处转移(尤其是肝和腹膜);其二,“铜墙铁壁”的肿瘤堡垒,胰腺癌肿瘤周围有致密的纤维结缔组织包裹,犹如一层“铠甲”,这导致化疗药物、靶向药物很难有效进入肿瘤内部发挥作用;其三:典型的“冷肿瘤”免疫微环境,胰腺癌肿瘤细胞及周边细胞会分泌大量抑制免疫的细胞因子和代谢产物,并调动调节性T细胞、肿瘤相关巨噬细胞等“帮凶”细胞发挥作用,它们非但不攻击癌细胞,反而会主动抑制杀伤性T细胞的功能,甚至帮助肿瘤生长和转移。
3、治疗的“绝望堡垒”。手术是唯一根治希望,但机会渺茫,只有不到20%的患者在确诊时有手术机会,且胰腺手术是普外科最复杂、并发症风险最高的手术之一;药物治疗效果有限,无论是传统化疗还是当下的新兴疗法,对胰腺癌的治疗效果都远不及其他癌种,耐药性也很快产生,即便是目前大获成功的PD-1/L1抑制剂等免疫检查点疗法,其原理是“松开”T细胞的刹车,但对于胰腺癌,由于肿瘤内部根本没有或只有极少的T细胞(即“无刹车可松”),这类药物单用几乎无效。
中国国家癌症中心发布的最新数据(J Natl Cancer Cent. 2024)显示,中国胰腺癌年新发病例数约为12万例,死亡病例数约为11万例,5年生存率约为7.2%,是所有主要恶性肿瘤中生存率最低的癌种。即使在全球范围内,胰腺癌也是被公认的生存率最低、预后最差的癌种之一。尽管近年来胰腺癌的基础研究与临床转化取得一定进展,但整体仍面临巨大挑战,现有化疗方案疗效已达瓶颈,靶向/免疫治疗仅覆盖极少数特定人群,亟需开发新的兼顾疗效和安全性的药物,以满足巨大的临床需求。
TCR-T方兴未艾:XLS-103注射液“一箭双雕”直面两大“癌王”
幸运的是,科学家们发现这两大“癌王”有共同的肿瘤靶点—KRAS突变。其中,由人类白细胞抗原HLA-A*A1101递呈的KRAS G12V更是符合中国人群的靶点,因为HLA-A*1101基因型是中国人群中占比最高的HLA-A亚型。作为一家中国的本土公司,该靶点自然也进入了香雪生命科学的视野,但启动一条新的管线不是儿戏,文章的数据有时候不一定能真的实现。据此,早在2016年,香雪生命科学就利用自主开发的抗原肽发现平台,在实验室里证实了这一靶点的真实性,然后便将其纳入公司的研发管线,与其它管线一道同步推进。
十年磨一剑,在生物医药的开发上体现的淋漓尽致。香雪生命科学牢记使命、不忘初心,终于在2025年12月22日,收到了国家药监局对不久前申报的针对KRAS G12V/HLA-A*1101的高亲和力TCR-T细胞治疗产品“XLS-103注射液”新药临床试验申请(IND)(受理编号为:CXSL2500856、CXSL2500857)的临床试验许可。更值得庆贺的是,该细胞治疗产品本次获批了两个适应症:
适应症1:用于治疗基因型为HLA-A*11:01,肿瘤新生抗原KRAS G12V突变阳性的晚期非小细胞肺癌。
适应症2:用于治疗基因型为HLA-A*11:01,肿瘤新生抗原KRAS G12V突变阳性的晚期胰腺癌。
正是上述的两位“癌王”。

“XLS-103注射液”是香雪生命科学第三款高亲和力TCR-T细胞治疗产品。与传统化疗、放疗“杀敌一千自损八百”的模式不同,TCR-T疗法具有特异性强、副作用小的优势,尤其在攻克实体瘤方面展现出独特潜力。TCR-T是通过基因工程技术,给人体自身的免疫T细胞装上“精准导航系统”(即T细胞受体,TCR),让原本“失灵”的免疫细胞能精准识别并杀死癌细胞,相当于为免疫系统打造了一支“精准制导的细胞导弹部队”。
随着本次两个适应症获批IND,香雪生命科学的三款TCR-T产品覆盖了软组织肉瘤、非小细胞肺癌、食管癌、肝癌、胃癌、胰腺癌等多个难治实体瘤,形成了梯度清晰、覆盖面广的研发管线布局。
Force, Lisa M et al. The global, regional, and national burden of cancer, 1990–2023, with forecasts to 2050: a systematic analysis for the Global Burden of Disease Study 2023. The Lancet. 2025 Zheng R, Zhang S, Zeng H, et al. Cancer incidence and mortality in China, 2022. Journal of the National Cancer Center. 2024 Sung H, Ferlay J, Siegel RL, et al. Global Cancer Statistics 2022: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin. 2024 Huang L, Guo Z, Wang F et al. KRAS mutation: from undruggable to druggable in cancer. Sig Transduct Target Ther .2021