
资讯中心
作者:张孟娟
发布时间:2026-03-05
阅读:1041
在人类与癌症的漫长抗争路上,RAS家族无疑是占据了战争的核心,不仅是因为在全球近五分之一的癌症中存在了RAS家族基因的突变,更是因为它能诱发最难治愈的胰腺癌、以及结直肠癌、非小细胞肺癌和多种实体瘤[1]。
1. RAS的发现
RAS在20世纪60年代被发现,起初是Jennifer Harvey发现一种能从大鼠体内提取并在小鼠中诱发肉瘤的病毒,随后Werner Kirsten也发现了另一株能在小鼠中诱发白血病的病毒,后被分别命名为Harvey murine sarcoma virus和Kirsten murine sarcoma virus。但随着癌基因理论的发展,人们意识到这并不是一种病毒,而是人类自身的基因,由此揭开了癌症可以由我们自身基因的突变引起,而不仅仅是外源病毒或环境因素影响的结果,而这些基因则被称为“原癌基因”。
2. RAS的研究进展
RAS家族主要有三个经典成员,分别是HRAS、KRAS和NRAS,它们在结构上具有高度的同源性,但分布和功能略有不同。HRAS和KRAS是从大鼠肉瘤急性反转录病毒中分离得到的,NRAS则是从人类神经母瘤细胞系中发现的。HRAS、KRAS和NRAS分别定位在人11号、12号和1号染色体上,三种RAS基因编码四种蛋白亚型:HRAS、KRAS4A、KRAS4B和NRAS[2]。
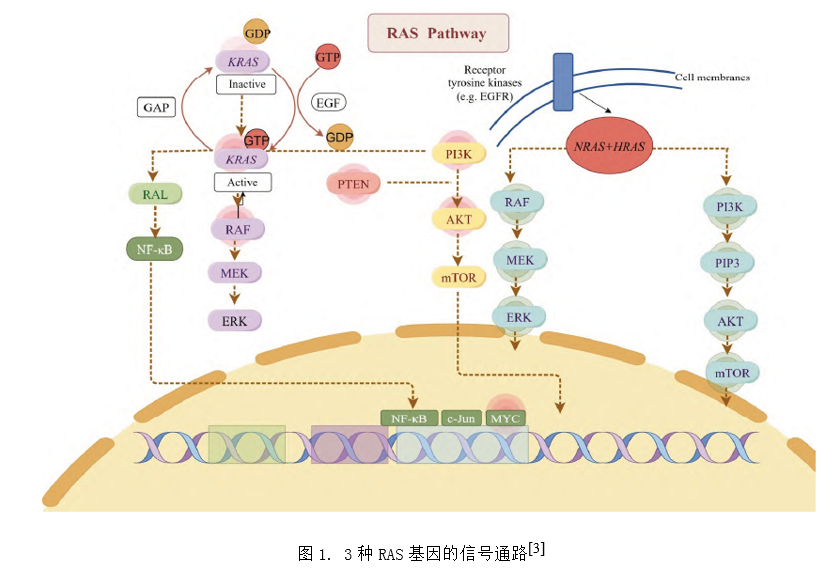
RAS作为一种小G蛋白,具有GTP水解酶活性,充当着细胞信号网络中的分子开关,RAS受到EGF的调控,促进GDP释放和GTP结合,激活下游RAF-MEK-ERK、PI3K-AKT及RAL信号通路,进而调控细胞信号转导,影响细胞增殖、分化和衰老等过程[4],像开启者;而GAP则加速GTP水解,像关闭者。RAS基因的突变使这一精巧的开关失灵,RAS对GAP的响应能力大大降低,导致开关“卡”在开启位置,即使没有外界生长信号,RAS也持续向下游发送增殖指令,驱动细胞持续生长形成肿瘤。在RAS的突变中(经常发生在第12、13或61位密码上),KRAS突变最常见于胰腺癌(PDAC; 86%)、结直肠癌(CRC; 41%)和非小细胞肺癌(NSCLC; 32%)[5];NRAS则在皮肤黑色素瘤和急性骨髓性白血病中较为常见;HRAS突变主要集中在膀胱癌以及头颈鳞状细胞癌[6]。
3. RAS相关药物的开发
自1982年RAS作为人类癌基因被确认后,在长达数十年的研究里,始终没有得到突破。RAS与其他激酶类癌蛋白不同,其表面异常光滑,缺乏明显的“口袋”或“裂缝”让小分子药物结合,同时它与其底物GTP/GDP的结合亲和力极高,几乎无法被竞争性抑制剂取代。更复杂的是,RAS需要定位到细胞膜内侧才能发挥作用,但针对这一过程的药物开发也困难重重。
最初科学家们将重点放在酶抑制剂上,企图通过利用抑制剂(法尼基转移酶)来阻止RAS蛋白定位在细胞膜上,然而在对癌症病人的治疗中却效果不佳,同时也发现,KRAS和NRAS可以利用其他修饰途径定位在膜上,从而绕过抑制作用[7];既然直接靶向看似不可行,那间接策略是否能成功,随后人们采取攻击RAS信号通路的下游节点的方式,效应蛋白RAF、MEK、ERK的抑制剂陆续被开发出来,但它们的疗效往往因为耐药性而受限。
随着技术的进步,多学科领域的交叉,在2013年,Kevan M. Shokat团队在nature上发表了关于KRAS G12C突变体的文章,打破了KRAS “不可成药”的教条,他们发现,G12C突变不仅在功能上使RAS持续激活,还在蛋白表面创造了一个全新的、可利用的“口袋”。基于此开发的新药(Sotorasib),最终在2021年在美国获批,用于治疗KRAS G12C突变的非小细胞肺癌患者。
直接抑制剂的成功为相关研究开辟了大门,针对KRAS G12C的胜利只是开始。RAS战场已经演变为多战线、多策略的全面战争,针对KRAS G12D(在胰腺癌和结直肠癌中常见)的抑制剂MRTX1133在临床前研究中显示出良好的效果[8],目前已进入早期临床试验,针对G12V、G13D等其他突变的药物也正在开发中;同时间接策略也在不断进化,新一代的SHP2抑制剂(SHP2是RAS上游的关键衔接蛋白)正在临床试验中测试,可能与直接RAS抑制剂产生协同作用[9];鉴于KRAS蛋白难以直接靶向, 合成致死策略被提了出来,两个或多个非致死性的基因同时缺陷导致肿瘤细胞死亡的现象即为合成致死,科学家已发现多个潜在的合成致死靶点,如STK33等,相关药物也正在开发[10];TCR-T技术则利用RAS突变会在癌细胞表面递呈新的抗原,从而能够被改造后的T细胞识别,达到精准治疗的目的,该策略同样是绕开了KRAS蛋白难以直接靶向问题,从细胞层面对肿瘤实施精准的“降维打击”,目前全球已有一款药物上市。
4. 展望
回顾RAS家族的研究历程,从病毒中的意外发现,到人类原癌基因的确认,再到长达四十年的“不可成药”困境,随后迎来靶向治疗的新时代。今天,细胞/基因治疗(CGT)已成为全球最受瞩目且最具潜力的癌症治疗方式,例如以CAR-T为代表的血液瘤细胞免疫治疗技术、以TCR-T为代表的实体瘤细胞免疫治疗技术,正在改写人类抗癌的治疗模式。这是一条充满曲折但最终走向光明的科学路径。随着更多靶向药物的开发、更多的细胞基因治疗产品的上市、更精准的组合策略的应用以及早期检测技术的进步,我们有理由相信,曾经令人绝望的RAS突变癌症,将逐渐转变为可管理、可控制甚至可治愈的慢性疾病。
参考文献 [1] Perurena N , Situ L , Cichowski K .Combinatorial strategies to target RAS-driven cancers[J].Nature Reviews Cancer, 2024, 24(5):22. [2] Malumbres M , Barbacid M .RAS oncogenes: the first 30 years.[J].Nature Reviews Cancer, 2003, 3(6):459-465. [3] 任佳宁,万扬,竺晓凡.RAS相关自身免疫淋巴细胞增殖性疾病诊疗进展[J].中国当代儿科杂志, 2025, 27(9):1149-1154. [4] Chen K , Zhang Y , Qian L ,et al. Emerging strategies to target RAS signaling in human cancer therapy[J].Journal of Hematology & Oncology, 2021, 14(1). [5] Moore, A. R., Rosenberg, S. C., McCormick, F. & Malek, S. RAS-targeted therapies: is the undruggable drugged? Nat. Rev. Drug. Discov. 19, 533–552 (2020). [6] Quinlan MP, Settleman J. Isoform-specific ras functions in development and cancer. Future Oncol 2009; 5(1): 105-16. [7] Ahearn IM, Haigis K, Bar-Sagi D, Philips MR. Regulating the regulator: post-translational modification of RAS. Nat Rev Mol Cell Biol 2011; 13(1): 39-51. [8] Wang X , Allen S , Blake J F ,et al.Identification of MRTX1133, a Noncovalent, Potent, and Selective KRASG12D Inhibitor[J].Journal of Medicinal Chemistry, 2022, 65(4) [9] Fedele C , Li S , Teng K W ,et al.SHP2 inhibition diminishes KRASG12C cycling and promotes tumor microenvironment remodeling[J].Journal of Experimental Medicine, 2021, 218(1). [10] Scholl C, Frohling S, Dunn IF, Schinzel AC, Barbie DA, Kim SY, et al. Synthetic lethal interaction between oncogenic KRAS dependency and STK33 suppression in human cancer cells. Cell 2009; 137(5): 821-34.